보령제약의 소세포폐암 신약
‘러비넥테딘(젭젤카)’의 희귀의약품 지정 신청으로
갑자기 희귀의약품에 대한 관심이 높아졌는데,
제약사들 입장에선 희귀의약품에 눈독을 들일 수 밖에 없는 이유가 있다.
먼저 희귀의약품이 무엇인지부터 살펴보면,
희귀의약품이란 적용대상이 드물고 적절한 의약품이 없어
긴급한 도입이 요구되는 의약품으로서,
「희귀의약품 지정에 관한 규정」에 정하여
고시한 의약품을 말한다.

1. 국내 환자수가 2만명 이하인 질환에 사용될 경우
2. 적절한 치료방법과 의약품이 개발되지 않은 질환에
사용하기 위해 개발하는 경우
3. 기존 대체 의약품보다 현저히 안전성
또는 유효성 개선이 예상되는 경우

허가의약품 뿐만이 아니라
임상시험단계나 비임상시험 단계의 경우에도
“개발단계 희귀의약품” 으로 지정이 가능하다.
위와 같은 조건을 만족한다고해서
자동적으로 희귀의약품으로 지정이 되는 것이 아니라,
희귀의약품으로 지정받기 위해서는
아래와 같은 희귀의약품 지정신청서와
구비서류를 첨부하여 식약처장에게 제출해야 한다.

유병률이 낮음에도 불구하고
제약사들은 희귀의약품에 눈독을 들일 수 밖에 없다.
먼저 법적인 부분부터 살펴보자.
국내에서 희귀의약품으로 지정이 되면
희귀질환관리법 제19조에 의해
약사법에 대한 특례를 받을 수 있다.

대표적인 특례를 자세히 살펴보면,

1. 신속심사를 신청할 수 있다!
: 치료적 확증 임상시험자료를 제출하는 것을 조건으로
탐색적 임상시험자료를 확증임상시험자료로 갈음할 수 있다.
즉 임상 3상 자료 제출을 조건으로,
임상2상 완료 후 허가신청을 할 수 있다는 의미!
2. 허가신청 시 안전성, 유효성에 관한 자료 일부 면제된다!
독성시험자료를 단회독성, 1-3개월 반복독성시험자료로,
약리자료를 효력시험자료 또는 임상자료로 갈음할 수 있다.

3. 재심사기간 연장!
타 신약의 재심사기간이 4~6년인 것에 반해,
희귀의약품은 재심사기간을 10년 부여 가능하다!
(소아 적응증을 추가하는 의약품에 대해서는
재심사기간 1년 연장이 추가된다!)
또한 법령에 명시되어있지는 않지만
재심사제도를 우회적으로 활용해
10년간 독점적 지위를 부여, 즉 시장독점권을 갖게 된다.
참고기사) http://www.newsmp.com/news/articleView.html?idxno=206452
4. 승인, 사전검토, 허가 신청 등 수수료 감면 혜택이 있다!
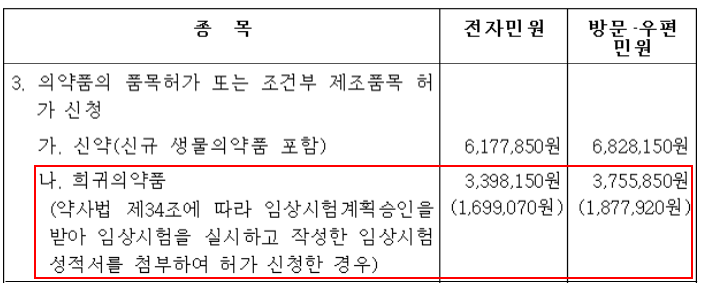
희귀의약품은 대상 환자수가 적어
임상시험의 기회도 적고 개발이 어려우나,
법적으로 다양한 혜택을 지원받고,
독점적지위와 재심사기간 이후에도
대체치료제 개발이 미흡한 경우가 많아
고가를 유지하는 경향이 있다.
이러한 이유로 고부가가치 영역으로 인식되고 있기 때문에
제약사들의 입장에서는 매력적인 시장일 수 밖에 없다:)
'소담한 스터디' 카테고리의 다른 글
| 임상시험에서 눈가림(Blinding)의 종류 (0) | 2020.07.24 |
|---|---|
| 임상시험에서 약물이상반응의 예측성(Expectedness) 평가 (0) | 2020.07.24 |
| 의약품 재심사 제도 (0) | 2020.07.21 |
| 의약품 시판 전/시판 후 안전성 정보 보고 (0) | 2020.07.07 |
| 임상시험 안전성정보 보고 관련 규정 정리 (0) | 2020.07.06 |




댓글