일반적으로 임상시험은 대상자 등록이 단기간에 이루어지며,
임상시험의 목적에 맞게
선정제외기준이 엄격하게 정해져 있어
이를 벗어나는 경우 임상시험 대상에서 제외될 수 밖에 없어,
치료기회를 부여하는 측면에서는 한계가 있다.
따라서 식약처에서는 임상시험계획 승인을 받은
임상시험용의약품에 한하여, 치료목적 사용을 허용하고 있다.
임상시험용의약품의 치료목적 사용은
다음과 같은 대상 질환에 대하여 사용이 승인된다.

임상시험용의약품의 치료목적 사용승인은
1. 개인별 치료목적 사용승인 과
2. 다수 환자 치료목적 사용승인 두 종류가 있다.
각각에 대해 자세히 살펴보자☺
1. 개인별 치료목적 사용승인

< 개인별 치료목적 사용승인의 주요 특징 >
- 개인별 치료목적의 경우 전문의가 신청을 하게 된다.
- 말기암 환자 등에 대해 치료기회 부여 차원에서 사용되므로
적응증이 반드시 임상시험과 일치하여야 하는 것은 아니다.
- 전문의 판단에 따라 임상시험용의약품 사용이
위험보다 이익이 더 크다고 판단하는 경우 사용할 수 있다.
- 해당 임상시험용의약품으로 진행된 임상시험에
참여한 의사가 아니어도 신청 가능하다.
- 국내에서 임상시험계획승인을 받은 바 있어야 하며,
임상시험의 진행 또는 종료여부와는 관계없이 신청 가능하다.
2. 다수 환자 치료목적 사용승인
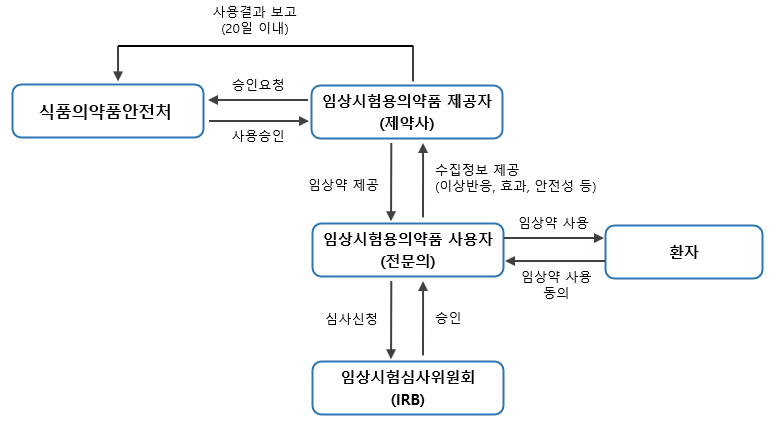
< 다수 환자 치료목적 사용승인의 주요 특징 >
- 임상시험을 통하여 임상적 효과가 관찰된
임상시험용의약품에 한하여 가능하다.
- 의약품 개발업체가 신청하며,
사용계획서를 제출하여야 한다.
- 임상시험실시기관의 IRB 승인을 받아야하며,
사용계획서에서 정하고 있는 환자만을
대상으로 사용해야 한다.
※ 참고
"치료목적 사용승인 시 해당 의약품이
아직 허가 전이라는 점을 고려하여 무상공급이 바람직하나,
최근 개발되는 의약품의 경우 제조비용이 높아
비용부담으로 인해 제약사가 의약품의 공급을 꺼리게 되어
환자 치료기회가 제한될 우려가 있다.
따라서 원가에 해당하는 비용을
예외적으로 청구할 수 있지만,
상업적 이용 등을 막기 위하여 엄격하게 산정하여
제조에 직접적으로 소요되는 비용만을 원가로 인정한다😊"
'소담한 스터디' 카테고리의 다른 글
| 임상시험 관련 보고 종류와 기한(임상시험 종료보고, 실시상황보고 등) (0) | 2020.09.18 |
|---|---|
| 적응적 설계 임상시험(Adaptive Design Clinical Trials) (0) | 2020.09.14 |
| 임상시험 형태별 설계유형(단일군 vs 평행설계 vs 교차설계 vs 요인설계) (0) | 2020.08.20 |
| 임상시험 비교유형별 설계(우월성시험 vs 비열등성시험 vs 동등성시험 vs 차이성시험) (0) | 2020.08.14 |
| 임상시험에서 분석대상군(Analysis Population Set) : ITT, FAS, PPS에 대하여 (0) | 2020.08.05 |




댓글