◈ 분석대상군(Analysis Population Set)
임상시험 자료의 분석 시 분석에 포함될 대상자군은
임상시험계획서에 미리 정의되어 있어야 한다.
무작위 배정 받은 모든 대상자가 모든 선정기준을 만족하고,
중도 탈락 없이, 시험과정 모두를 완벽하게 실시하여
자료가 완벽하게 기록되어있다면
모든 시험대상자에 대해 분석을 하는 것이 이상적이겠지만,
실제 대부분의 임상시험 시, 수행 과정 중
계획서 위반이나 중도탈락 사례가 빈번하게 발생한다.
따라서 이러한 예상 문제점들이 자료 분석에
어떠한 영향을 미치는지에 대해 미리 명시해 놓아야하고,
자료분석 과정에서 발생하는 문제들을 최소화하기 위한
방법이 구체적으로 기재되어있어야한다.
분석대상군의 정의는 ICH가이드라인 E9에 따라
ITT원칙을 기본으로 한다.
* ITT원칙(Intention-To-Treat principle)
ITT 원칙은, 중도탈락된 대상자까지 포함해서
무작위 배정된 대상자를
모두 분석에 포함시켜야 한다는 것이다.
또한 무작위 배정된 모든 대상자는
처음 배정된 치료군에 속한 것으로 하여
(비록 투약이 잘못되었더라도 처음 배정군으로 취급)
분석을 시행해야 한다는 원칙이다.
즉, ITT원칙에 따르면, 모든 대상자는
계획된 치료에 순응하는지 여부와는 상관없이
처음 배정된 군의 구성원으로 추적관찰되고,
평가되고, 분석되어야 한다.
임상시험을 진행하는 의뢰사의 입장에서 언뜻 들으면
너무 보수적이고 불합리적이라고 생각될 수 있으나,
실제 진료상황에서는
예상치 못한 다양한 상황이 발생할 수 있으므로
실체 치료효과의 참값에 가장 가까운 값이라고 볼 수 있다.
분석군은 크게 세가지로 분류된다.
FAS, PPS, Satety Set.
1. FAS(Full Analysis Set)
FAS 분석군은 ITT 원칙의 개념과 가장 근접하면서,
이상적인 연구대상 집단으로,
무작위 배정된 대상자 중 제외사유가 정당한
최소한의 대상자들을 제외한 분석군이다.
정당한 제외사유에는 다음과 같은 사유가 있다.
- 주요한 선정기준을 위반한 경우
- 등록 후 임상시험용 의약품을 단 한번도 투여받지 못한 경우
- 무작위 배정 이후의 자료가 전무한 경우
FAS 분석군은 결측치가 발생할 수 있으므로
결측치 처리를 어떻게 진행할지 임
상시험계획서에 기술되어있어야 한다.
2. PPS(Per Protocol Set)
FAS에 포함되는 대상자 중 계획서를 잘 순응하여
연구를 종료한 임상시험 대상자들로 정의할 수 있다.
PPS 분석군에 해당하는 예)
- 미리 정한 최소 기간 이상의 치료를 완료한 경우
- 주 결과변수의 측정치를 이용할 수 있는 경우
- 선정기준을 포함하여 임상시험계획서의
주요한 기준을 위반하지 않은 경우 등
PPS 분석군에서 제외되는 오류의 예)
- 무작위배정 오류, 병용금지약물의 사용,
대상자의 낮은 순응도, 추적관찰 실패, 결측치 발생,
기타 임상시험계획서 위반 등이 있다.
3. Safety Set
Safety Set 분석군은 무작위 배정된 이후
임상시험용의약품이나 의료기기를
단 한번이라도 복용하거나 처치를 받은
모든 대상자들이 포함된다.
예를 들어 살펴보자.
만약 신약과 대조약 비교 임상시험이
아래와 같이 진행되었을 경우,
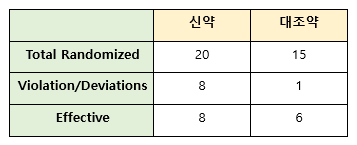
PPS 분석군에는 Violation/Deviations 대상자는 제외된다.
따라서
* 분석군을 PPS로 정의했을 경우
신약의 유효성 : 8/12 = 0.67
대조약의 유효성 : 6/14 = 0.43
임상시험의 결론 : 신약이 대조약보다
효과가 좋다고 할 수 있음.
* 분석군을 FAS로 정의했을 경우
신약의 유효성 : 8/20 = 0.40
대조약의 유효성 : 6/15 = 0.40
임상시험의 결론 : 신약과 대조약이 동등한 효과를 보임.
이처럼 분석군을 어떻게 정의하느냐에 따라
임상시험의 결과가 달라질 수도 있기때문에
임상시험에서 분석군을 정의하는 것은 매우 중요하다.
또한 임상시험이 종료된 후 분석군을 정하게 되면
임상시험의 결과에 따라 유효성을 높이기 위한 방향으로
분석군을 정하게 될 수도 있는데
이는 임상시험의 신뢰도를 떨어뜨릴 수 있으므로
분석군 정의는 임상시험계획에 포함되어있어야 한다.
'소담한 스터디' 카테고리의 다른 글
| 임상시험 형태별 설계유형(단일군 vs 평행설계 vs 교차설계 vs 요인설계) (0) | 2020.08.20 |
|---|---|
| 임상시험 비교유형별 설계(우월성시험 vs 비열등성시험 vs 동등성시험 vs 차이성시험) (0) | 2020.08.14 |
| 식약처 의약품 정책설명회-① 제네릭의약품 GMP관리 강화 방안 (1) | 2020.08.04 |
| ALCOA-C 원칙(데이터 무결성의 원칙) (0) | 2020.07.28 |
| 임상시험에서 눈가림(Blinding)의 종류 (0) | 2020.07.24 |




댓글